Chercheurs et cliniciens impliqués : Christophe Breton
a/ L’identification de cibles épigénômiques au cours du développement
Les changements de mode de vie, en particulier la consommation excessive d’aliments à forte densité énergétique et une activité physique insuffisante, sont les moteurs de l’épidémie mondiale d’obésité et de complications métaboliques. L’hypothèse de l’origine développementale de la santé et de la maladie (Dohad) suggère que les environnements défavorables, soit in utero, soit au début des périodes de développement postnatal, entraînent une programmation délétère à long terme du métabolisme.
Christophe Breton (PU en physiologie à l’Université de Lille) a rejoint notre équipe en 2020. Son équipe a précédemment rapporté chez les rongeurs qu’un régime maternel riche en graisses pendant la gestation ainsi que la lactation induisent une altération morphologiques et transcriptionnelle du tissu adipeux chez la descendance adulte via des modifications épigénétiques au cours du développement, en particulier la méthylation et l’hydroxyméthylation de séquences spécifiques / ciblées de l’ADN.
Grâce à l’utilisation de modèles murins, cela a permis de mettre en évidence que des marques épigénétiques spécifiques sont programmées par l’obésité maternelle, associée à une tolérance au glucose altérée, à une résistance à l’insuline et à une détérioration de la sécrétion d’insuline avec des modèles d’expression génique spécifiques chez les futurs enfants adultes sujets au DT2. Chez les rongeurs, la maturation du tissu adipeux se finalise lors de la gestation et de la lactation.
Ainsi, nous postulons que les cellules adipeuses sont au cœur de la programmation métabolique, et que l’obésité maternelle pourrait provoquer une résistance à l’insuline chez la descendance via des mécanismes moléculaires précoces liés à l’épigénétique.
En utilisant un modèle murin d’obésité maternelle induite par un régime riche en graisses, nos objectifs sont:
- analyser l’architecture (c.-à-d. Taille, vascularisation, prolifération, apoptose, remodelage) et la fonction (c.-à-d. Synthèse et sécrétion d’adipokine, signalisation de l’insuline, lipogenèse) et lipolyse) des adipocytes des progénitures à différents stades postnatals de la lactation à l’âge adulte
- analyser simultanément les profils de transcriptome par RNA-seq, suivi d’une analyse bioinformatique des voies moléculaires pour déterminer les voies ciblées par la programmation du tissu adipeux
- corréler les changements du profil transcriptionnel de l’expression génique avec la méthylation de l’ADN (hydroxy) et les modifications d’histone (H3K27ac / H3K4me1 / H3K27me3) présentes dans les régions activatrices / promotrice. Outre la découverte de nouvelles cibles, ce projet pourrait constituer la première étape vers le développement de stratégies d’intervention pendant la période périnatale pour atténuer les effets de programmation délétères de l’obésité maternelle sur le tissu adipeux de la progéniture
b/ Combattre la résistance à l’insuline grâce au brunissement du tissu adipeux
Chez les rongeurs, les gènes qui empêchent l’accumulation de graisse et protègent contre l’obésité induite par l’alimentation et le DT2, tels que E2f1 et Sertad2 (TRIP-Br2), améliorent l’action de l’insuline dans la plupart des organes métaboliquement actifs, y compris le tissu adipeux.
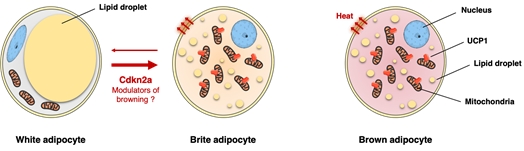
Les tissus adipeux comprennent les adipocytes blancs (WAT), bruns (BAT) et beiges. Les WAT stockent l’excès d’énergie sous forme de graisse et libèrent des acides gras libres (AGL) comme substrat énergétique. Les BAT et adipocytes beiges catabolisent les graisses, ce qui contribue à réduire les AGL circulants. Dans l’obésité, un taux élevé d’AGL circulants est associé à une résistance à l’insuline et au DT2. L’augmentation de la dépense énergétique par l’activation des BAT ou en favorisant le brunissement du WAT est récemment apparue comme une présumée nouvelle thérapie pour le DT2.
Chez l’homme, il existe également des arguments en faveur d’un rôle physiologique des adipocytes bruns / beiges pour améliorer la tolérance au glucose et la sensibilité à l’insuline. Par conséquent, l’élucidation des voies moléculaires impliquées dans la biogenèse des adipocytes beiges représenterait une première étape vers des traitements innovants (Figure 3).
Figure 3: le brunissement du tissue adipeux comme nouvelle stratégie pour le traitement de l’insulino-résistance et l’obésité.
Nous avons démontré que la délétion génétique de Cdkn2a favorise la dépense énergétique et améliore la sensibilité à l’insuline pendant l’obésité induite par le régime alimentaire grâce au contrôle du développement des adipocytes beiges. Ces données suggèrent que Cdkn2a joue un rôle clé dans le métabolisme énergétique en régulant une transition des graisses blanche à brune.
En outre, nous avons observé que les niveaux de CDKN2A étaient augmentés dans les adipocytes obèses humains, renforçant davantage CDKN2A en tant que cible potentielle dans l’obésité et le DT2.
En collaboration avec l’équipe du Dr Christian Dani (Institut de biologie de Valrose, Nice), nous déchiffrons actuellement la signature moléculaire suite à la reprogrammation des adipocytes bruns dérivés de cellules souches pluripotentes induites humaines déficientes en CDKN2A. En utilisant des cellules souches pluripotentes humaines induites (hIPSC) différenciées en adipocytes bruns, nous identifierons les voies de signalisation qui contribuent à cet effet métabolique à l’aide d’approches génomiques (RNA-seq / ChIP-seq) et de kinome entier (Pamgene.com) développées par notre équipe.
Notre deuxième objectif est d’évaluer les effets métaboliques des hIPSC transplantés dans des modèles murins de DT2 et d’obésité. Nos résultats actuels montrent que la diminution de l’expression de CDKN2A des cellules souches pluripotentes induites humaines (hIPSCs) par siRNA entraine une augmentation de l’expression d’UCP1. Cela suggère que ces cellules pourraient être pertinentes pour corriger les paramètres métaboliques pendant l’obésité.
Publications majeures associées de l’équipe :
– Lecoutre S., Oger F., Pourpe C., Butruille L., Marousez L., Dickes-Coopman A., Laborie C., Guinez C., Lesage J., Vieau D., Junien C., Eberlé D., Gabory A., Eeckhoute J., Breton C. (2017). Maternal obesity programs increased leptin gene expression in rat male offspring via epigenetic modifications in a depot-specific manner. Mol. Metab. 6(8): 922-930.
– Lecoutre S., Pourpe C., Butruille L., Marousez L., Laborie C., Guinez C., Lesage J., Vieau D., Eeckhoute J., Gabory A., Oger F., Eberlé D., Breton C. (2018). Reduced PPAR expression in adipose tissue of male rat offspring from obese dams is associated with epigenetic modifications. FASEB 32(5): 2768-2778.
– Lecoutre S., Petrus P., Rydén M., Breton C. (2018). Transgenerational epigenetic mechanisms in adipose tissue development. Trends Endocrinol. Metab. 29: 675-685.
– Rabhi N., Hannou S.A., Gromada X., Salas E., Yao X., Oger F., Carney C., Lopez-Mejia I.C., Durand E., Rabearivelo I., Bonnefond A., Caron E., Fajas L., Dani C., Froguel P., Annicotte J.S. (2018). Cdkn2a deficiency promotes adipose tissue browning. Mol. Metab. 8:65-76.
– Kahoul Y., Oger F., Montaigne J., Froguel P., Breton C*., Annicotte J.S.* (2020). Emerging roles for the INK4a/ARF (CDKN2A) locus in adipose tissue: Implications for obesity and type 2 diabetes. Biomolecules. 10(9): 1350 (*co-last author).